主要職責
中國科學(xué)院貫徹落實黨中央關(guān)于科技創(chuàng)新的方針政策和決策部署,在履行職責過程中堅持黨中央對科技工作的集中統(tǒng)一領(lǐng)導(dǎo)。主要職責是:
一、開展使命導(dǎo)向的自然科學(xué)領(lǐng)域基礎(chǔ)研究,承擔國家重大基礎(chǔ)研究、應(yīng)用基礎(chǔ)研究、前沿交叉共性技術(shù)研究和引領(lǐng)性顛覆性技術(shù)研究任務(wù),打造原始創(chuàng)新策源地。 更多+
院況簡介
中國科學(xué)院是國家科學(xué)技術(shù)界最高學(xué)術(shù)機構(gòu)、國家科學(xué)技術(shù)思想庫,自然科學(xué)基礎(chǔ)研究與高技術(shù)綜合研究的國家戰(zhàn)略科技力量。
1949年,伴隨著新中國的誕生,中國科學(xué)院成立。建院70余年來,中國科學(xué)院時刻牢記使命,與科學(xué)共進,與祖國同行,以國家富強、人民幸福為己任,人才輩出,碩果累累,為我國科技進步、經(jīng)濟社會發(fā)展和國家安全作出了不可替代的重要貢獻。 更多+
院領(lǐng)導(dǎo)集體
機構(gòu)設(shè)置
科技獎勵
科技期刊
科技專項
科研進展/ 更多
工作動態(tài)/ 更多
工作動態(tài)/ 更多
中國科學(xué)院學(xué)部
中國科學(xué)院院部

語音播報

阿爾茨海默病中,神經(jīng)細胞內(nèi)磷酸化Tau蛋白(p-Tau)的異常聚集與神經(jīng)退行性病變相關(guān)。同時,大腦葡萄糖代謝降低是預(yù)測認知功能障礙的重要臨床指標。一個如同纏住神經(jīng)元的“結(jié)”,一個好似掐斷能量供給的“閘”,但這兩個特征如何協(xié)同作用并共同驅(qū)動阿爾茨海默病進程,仍是尚未闡明的問題。
近日,中國科學(xué)院上海有機化學(xué)研究所等,揭示了葡萄糖代謝降低與p-Tau協(xié)同作用,通過調(diào)控RIPK1介導(dǎo)的程序性壞死通路,驅(qū)動阿爾茨海默病發(fā)生發(fā)展的分子機制。
體外細胞實驗與體內(nèi)動物模型研究表明,葡萄糖代謝降低與p-Tau并非獨立發(fā)揮作用,而是形成協(xié)同效應(yīng),共同誘導(dǎo)神經(jīng)元程序性壞死并導(dǎo)致神經(jīng)元丟失。在低濃度葡萄糖環(huán)境下,異常積累的p-Tau可作為功能性分子支架,直接招募程序性壞死關(guān)鍵激酶RIPK1。同時,程序性壞死檢查點蛋白A20表達下調(diào),削弱其對該通路的負向調(diào)控作用,從而解除對細胞死亡的抑制。
這一“協(xié)同調(diào)控”機制共同促進神經(jīng)元程序性壞死。在干預(yù)層面,補充乙酰左旋肉堿恢復(fù)A20表達,或利用RIPK1中間結(jié)構(gòu)域來源的肽段,阻斷p-Tau與RIPK1的相互作用,均可在Tau轉(zhuǎn)基因小鼠模型中抑制神經(jīng)元程序性壞死,減輕腦萎縮,并緩解學(xué)習(xí)記憶功能損傷。
該研究揭示了一條由p-Tau–RIPK1軸介導(dǎo)的代謝驅(qū)動型程序性壞死機制,為理解大腦葡萄糖代謝與Tau病理之間的功能聯(lián)系提供了依據(jù),并為阿爾茨海默病的干預(yù)策略提供了新思路。
相關(guān)研究成果在線發(fā)表在《神經(jīng)元》(Neuron)上。研究工作得到國家自然科學(xué)基金委員會和中國科學(xué)院等的支持。
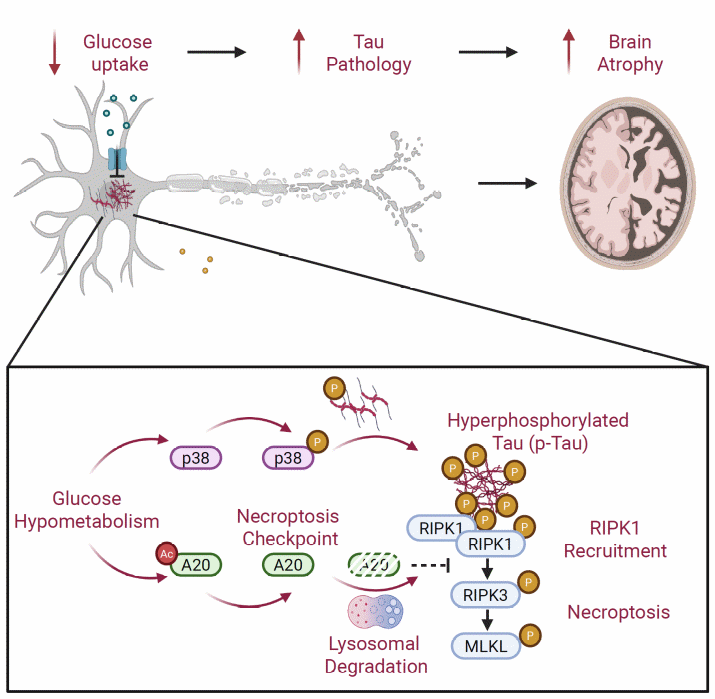
葡萄糖代謝降低與p-Tau協(xié)同驅(qū)動神經(jīng)元程序性壞死的作用機制示意圖

© 1996 - 中國科學(xué)院 版權(quán)所有 京ICP備05002857號-1  京公網(wǎng)安備110402500047號 網(wǎng)站標識碼bm48000002
京公網(wǎng)安備110402500047號 網(wǎng)站標識碼bm48000002
地址:北京市西城區(qū)三里河路52號 郵編:100864
電話: 86 10 68597114(總機) 86 10 68597289(總值班室)














